.jpg)
crédit image: NASA
OCÉANS
Sébastien Lauwers
20 Octobre 2020
Update : 21 Mars 2021
Prologue
il y a environ 1 385 millions de kilomètres cubes d'eau sur Terre et - sauf accident - nous n'en aurons pas une goutte de plus. C'est un cycle fermé. Dans l'hydrosphère, les océans sont le véritable moteur du comportement en surface de la planète, et les météorologues traitent de plus en plus les océans et l’atmosphère comme un système unique. 97 % de toute l'eau sur Terre se trouve dans les océans, le Pacifique qui couvre la moitié de la planète avec 51,6 % de toute l'eau des océans, l'Atlantique 23,6 % et l'océan Indien 21,2 %. Le solde - 3,6 % - restant étant distribué entre les autres mers. L'essentiel des 3 % d'eau douce est contenue dans les banquises et une fraction minuscule - 0,036 % - dans les lacs, les rivières et nappes phréatiques, et une part encore plus infime sous forme de nuages ou de vapeur - 0,001%.
Les océans ne sont pas une masse d’eau uniforme.
Leurs différences de température, de salinité, de profondeur et de densité ont des effets impressionnants sur leur capacité à déplacer la chaleur, ce qui en retour affecte le climat. L’Atlantique, par exemple, est plus salé que le Pacifique, ce qui est une bonne chose. L’eau plus salée est plus dense, et l’eau dense coule. Sans cette charge supplémentaire de sel, les courants atlantiques remonteraient jusqu’en Arctique, réchauffant le pôle Nord mais privant l’Europe de toute sa bonne chaleur.
L’eau est excellente pour conserver et transporter la chaleur. Chaque jour, le Gulf Stream apporte à l’Europe une quantité de chaleur équivalente à dix ans de production de charbon dans le monde ; c’est pourquoi la Grande-Bretagne et l’Irlande ont un climat si tempéré par rapport au Canada et à la Russie. Mais l’eau se réchauffe lentement, ce qui explique que les lacs et les piscines restent froids, même aux jours les plus chauds. Un autre exemple est l’écart entre le début officiel d’une saison et la réalité astronomique (météo france 2020). Le principal agent de transfert de chaleur sur terre est ce que l’on appelle la circulation thermohaline, qui prend sa source dans les courants lents et profonds bien loin sous la surface – un processus détecté d’abord par l’aventurier scientifique von Rumford en 1797 (Hay, science 1993). Ce qui se passe, c’est qu’en s’approchant de l’Europe les eaux de surface se font plus denses, plongent à de grandes profondeurs et entament un lent voyage de retour vers l’hémisphère Sud. Quand elles atteignent l’Antarctique, elles sont prises dans le courant antarctique circumpolaire, qui les pousse dans le Pacifique. Le processus est très lent – l’eau peut mettre 1 500 ans à passer de l’Atlantique Nord au Pacifique, mais les volumes de chaleur et d’eau qu’il déplace sont considérables, et l’influence sur le climat est énorme. (Quant à savoir comment on a pu calculer le temps que met une goutte d’eau pour passer d’un océan à l’autre, la réponse est que les scientifiques peuvent mesurer des composants présents dans l’eau, les chlorofluorocarbures par exemple, et calculer le temps écoulé depuis qu’ils étaient dans l’atmosphère.
En recoupant diverses mesures en des lieux et des profondeurs différents, ils peuvent raisonnablement retracer les mouvements de l’eau). Outre qu’elle déplace la chaleur, la circulation thermohaline contribue aussi à mélanger les nutriments grâce aux mouvements des courants, rendant de plus grands volumes de l’océan habitables pour les poissons et autres créatures marines. Il semble malheureusement que cette circulation soit elle aussi très sensible au changement.
Des milliards et des milliards de minuscules organismes marins – foraminifères, coccolithes, algues calcaires et autres microbes marins (Worden 2015) – capturent le carbone de l’atmosphère sous forme de dioxyde de carbone quand il tombe en pluie, et s’en servent (combiné à d’autres éléments) pour fabriquer leurs coquilles. En enfermant ainsi le carbone dans leurs coquilles, ils l’empêchent de s’évaporer dans l’atmosphère, où il pourrait s’accumuler dangereusement en tant que gaz à effet de serre. Enfin, tous les foraminifères, coccolithes, etc., meurent et tombent au fond de la mer, où ils sont compressés sous forme de calcaire. Quand vous regardez les falaises de Douvres, songez qu’elles sont exclusivement constituées d’organismes marins, et songez aussi à la quantité de carbone qu’elles séquestrent à elles seules. Un centimètre cube de cette craie peut contenir des centaines de litres de dioxyde de carbone compressé qui ne nous ferait aucun bien s’il se trouvait à l’air libre. Au total, il y a environ vingt mille fois plus de carbone dans les roches terrestres que dans l’atmosphère. Une grande partie de ce calcaire finira par aller nourrir les volcans, et le carbone retournera dans l’atmosphère avant de retomber sur terre sous forme de pluie (Honjo 1997 - Bauer & al. 2013)
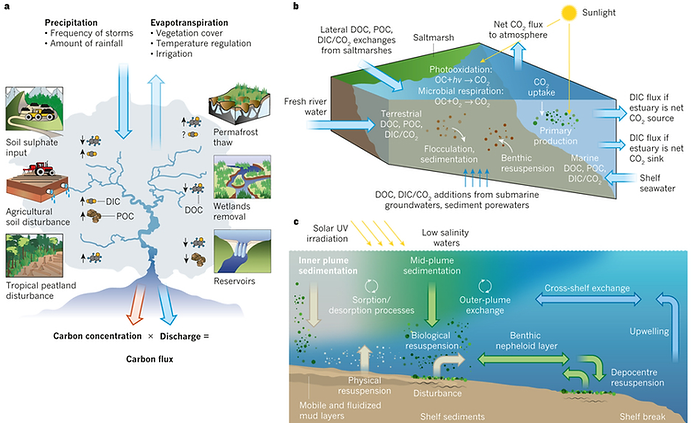
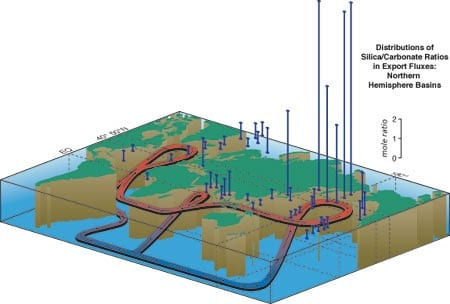
Le cycle du carbone saisonnier ( voire courbe de Keeling) montre une variation saisonnière d'environs 6ppmv avec un maximum en mai et un minimum en septembre qui reflète principalement la croissance et la respiration des plantes terrestres. La photosynthèse est la réaction de la matière organique à partire du dioxyde de carbone, de l'eau et des sels nutritifs (ions nitrates NO3 - et de phosphates PO4³-) sous l'effet de rayonnement solaire :
CO2 + H2O + rayonnement solaire (photon hv) --> [CH2O] + O2
ou l'élément chimique [CH2O] est juste une combinaison représentant les carbohydrates, le constituant de la matière organique. Les plantes absorbent le dioxyde de carbone et fabriquent de la matière organique et de l'oxygène sous l'effet du rayonnement solaire (visible). Comme les êtres vivants respirent, la réaction inverse de respiration (et combustion) a aussi lieu :
[CH2O] + O2 --> CO2 + H2O + énergie
Dans ce sens la réaction chimique produit de l'énergie qui permet à l'organisme de se mouvoir, se chauffer,... (le métabolisme des êtres vivants brûle de la matière organique, par exemple). Si l'on regarde l'ensemble des 2 réactions, il n'y a pas de production ou de consommation nette de CO2 ou d'oxygène mais juste une transformation d'énergie solaire en énergie mécanique. Comme le fonctionnement de ces réactions chimiques exige la présence d'oxygène, se pose la question de savoir comment l'oxygène est arrivé en premier lieu dans l'atmosphère.
Courte explication : en premier la matière organique fabrique de l'oxygène et ensuite l'organisme disparaît, enterré ou au mieux immergé avant que l'oxydation de la matière à l'air libre ne se produise par réaction inverse. L'oxygène a alors commencé à envahir, progressivement, il y a quelque 2,3 Mds d'années. Le maintien de l'oxygène à sa concentration actuelle nécessite que la production par photosynthèse, la disparition et l'oxydation de la matière organique s'équilibrent mutuellement. (Redfiels & al. 1958 - Martiny & al. 2014)
La réaction de photosynthèse existe bien sur aussi dans l'océan avec quelques spécificité. La création de matière organique se déroule près de la surface, car l'eau présente une forte opacité au rayonnement solaire et la lumière pénètre très mal. L'épaisseur de la couche éclairée, appelée euphorique, est de l'ordre d'une centaine de mètres dans les eaux claires des gyres tropicaux, mais est beaucoup plus faible dans les eaux côtières plus turbides, ce qui limite la disponibilité des photons. La couche de surface océanique est remplie de micro algues - le phytoplancton - de taille allant de 1 à 100 microns. Ces plantes utilisent un pigment - la chlorophylle - pour collecter les photons et ainsi produire de la matière organique. En allant des tropiques vers les hautes latitudes, la couleur de la mer passe du bleu clair au vert opaque, c'est cette variation qui traduit directement l'abondance de phytoplancton dans la couche euphotique. C'est cette abondance qui traduit la fonction du forçage solaire, mais aussi des sels nutritifs disponibles, de la température, de prédateurs.
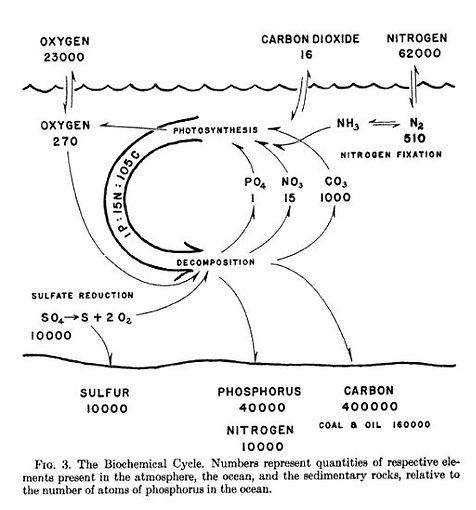
Le CO2 absorbé par l'eau de mer augmente chimiquement son pH (potentiel hydrogène) - son acidité. Au XIIIème siècle, le pH de l'eau était en moyenne de 8,25, en 1992 il a été mesuré à 8,11 et 2016 à 8,06, soit plus de 40 % depuis l'ère industrielle, ce qui est environ 100 fois plus rapide que tout changement d'acidité observé au cours des 55 derniers millions d'années (Rhein et al., 2013) . Les données proviennent de la série chronologique du pH de la station Aloha (adapté de Dore, JE, et al., 2009,).
Les changements ici sont similaires à ceux observés sur une période plus courte en Europe

Bien que le pH des océans ait varié dans le passé géologique, les paléo-événements ne sont peut-être que des analogues imparfaits des conditions actuelles. En effet, le potentiel d'adaptation des organismes marins à l'augmentation du CO2 et les implications plus larges pour les écosystèmes océaniques ne sont pas bien connus; les deux sont de grandes priorités pour les recherches futures. (Doney & al. 2009) En 2013 une étude (Bopp & al.) montre que l'augmentation constante et rapide du dioxyde de carbone atmosphérique (CO2), réduit le pH des océans et provoque des changements importants dans la chimie des carbonates de l'eau de mer. L'acidification modifie la spéciation chimique de l'eau de mer et les cycles biogéochimiques de nombreux éléments et composés. Un effet bien connu est l'abaissement des états de saturation en carbonate de calcium, qui affecte les organismes marins formant des coquillages, du plancton aux mollusques benthiques, échinodermes et coraux. De nombreuses espèces calcifiantes présentent des taux de calcification et de croissance réduits dans les expériences de laboratoire sous haute teneur en CO2. L'acidification des océans entraîne également une augmentation des taux de fixation du carbone dans certains organismes photosynthétiques (à la fois calcifiants et non calcifiants).
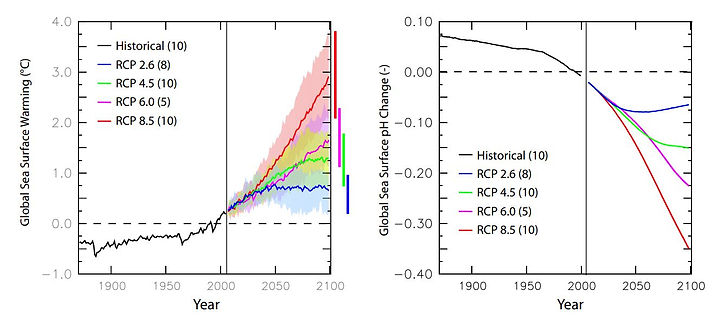
Impact des Forçages radiatifs sur les océans
Depuis 1850, on estime que nous avons envoyé environ 100 milliards de tonnes de carbone dans l’air, chiffre qui augmente de 7 Mds chaque année. La nature envoie +- 200 Mds de tonnes de gaz carbonique dans l'atmosphère chaque année – surtout par les volcans (activités 2021). En effet, les effets climatiques des éruptions volcaniques explosives comprend de nombreux processus chimiques et physiques qui conduisent à la formation d'aérosols volcaniques. Les aérosols volcaniques sont de minuscules particules en suspension dans l'air (fig 3.a) qui sont importantes pour le climat de la Terre car elles réfléchissent la lumière du soleil et piègent l'énergie radiative infrarouge thermique. plusieurs études prescrivent d'intégrer les effets des forçages radiatifs pour mesurer efficacement la température de la surface de la mer SST (Forster et al. 2016 - Zhang et al. 2014)
Ci dessous le graphique montre que les éruptions les plus puissantes entre 1979 et 2015 ont eu un effet rafraîchissant sur les températures (Schmidt & al. 2018).
Nous savons par des carottes de glace très ancienne que le niveau « naturel » de dioxyde de carbone dans l’atmosphère – avant que nous ne commencions à le gonfler par nos activités industrielles – est d’environ 280 ppm. En 1958, quand les scientifiques commencèrent à s’y intéresser, ce taux était monté à 315 par million. De nos jours, il est de l’ordre de 410 ppm et il s’accroît d’environ 0,25 % par an. lorsque l’on prend l'ensemble des forçages radiatifs - positifs et négatifs - augmentent l'impact du rayonnement solaire à une moyenne de +2,3 W/m². Il y a un seuil critique où la biosphère naturelle cesse de faire tampon à nos émissions et se met à les amplifier, la rétroaction.

Les rétroactions
Un réchauffement ou un refroidissement dû à un forçage externe modifie certaines composantes du système climatique. En fait, les mécanismes de rétroactions sont une réponse du climat aux forçages externes, amplifié par le forçage initial:
Amplification - rétroaction positive
Atténuation - rétroaction négative
les principales sources de rétroactions proviennent de changements physiques dans:
La circulation océanique, qui redistribue la chaleur dans l'ensemble du système climatique et sur la composition de l'atmosphère pour maintenir un équilibre des pressions entre l'océan et l'atmosphère. Ces changements affectent la chaleur et la composition atmosphérique et ont un impact sur la formation des eaux profondes (principalement l'Atlantique Nord), la modification du Gulf Stream --> rétroactions positives.
n.a.: Lorsque le climat se refroidit, lors d'une période glaciaire par exemple, des modifications induisent une diminution de l'apport calorifique aux moyenne latitudes ,en atlantique Nord, et entraîne une baisse de CO2.
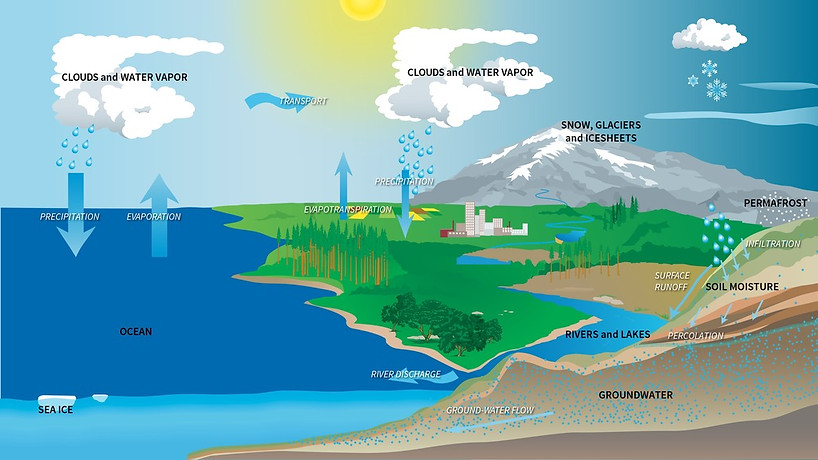
La biosphère, à travers la couverture végétale. Celle-ci affecte la reflection du rayonnement solaire, la verdure réfléchit moins qu'un sol nu. La biosphère joue aussi un rôle sur le cycle de l'eau par évapotranspiration (fig 1), ainsi que le cycle du carbone en le stockant dans la matière organique. Lors d'un réchauffement climatique la réponse de la biosphère répond en faisant remonter les régions boisées encore plus haut vers le Nord et en remplaçant progressivement la toundra ce qui a pour effet de diminuer la réflexion du rayonnement solaire et contribue à l'amplification du réchauffement --> rétroactions positives.
le cycle du carbone,
Ce processus prend très longtemps – environ un demi-million d’années pour un atome de carbone typique – mais en l’absence de toute autre perturbation il est remarquablement efficace pour assurer la stabilité du climat. le graphique ci dessous représentent les réservoirs de carbone en pétagrammes de carbone (PgC; 10 15 gC) et les échanges annuels en PgC / an. Les nombres noirs et les flèches montrent les réservoirs et les flux préindustriels. Les chiffres rouges et les flèches montrent les flux anthropiques supplémentaires calculer sur la période 2000-2009 (IPCC 2014) (graphique).
Le cycle de l'eau, dont les trois premières sources sont: l'état gazeux (vapeur d'eau) dans l'atmosphère, l'état liquide (les nuages) aussi dans l'atmosphère et l'état solide (neige ou glace) sur la surface terrestre.
La quatrième source est en relation avec des changements dans le transfert d'énergie entre la surface et l'atmosphère au travers du cycle de l'eau, appelé "lapse rate" (gradient de températures). Chacun de ses états amplifie ou atténue le changement.
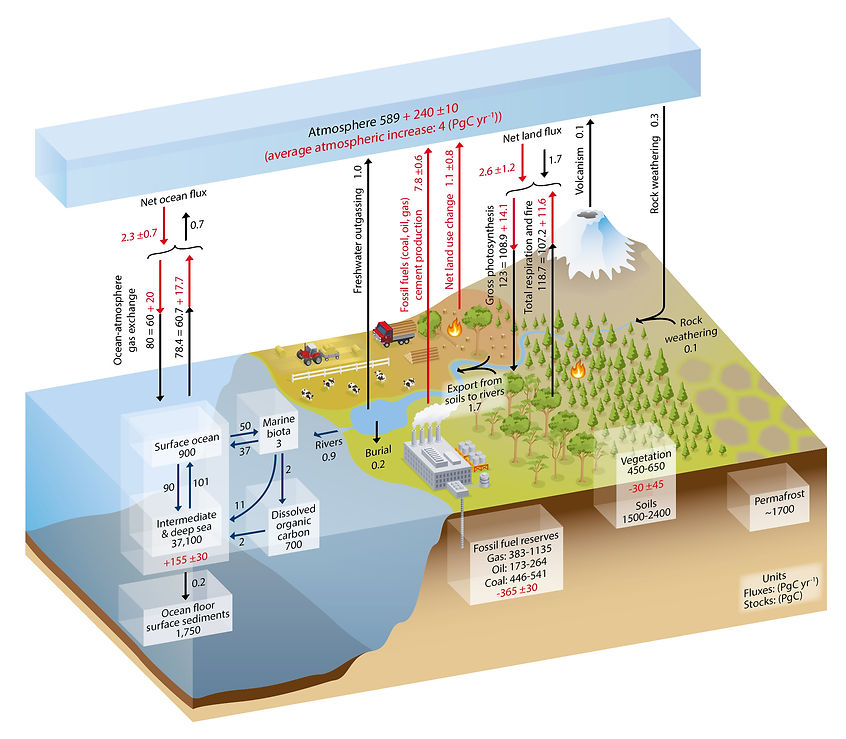
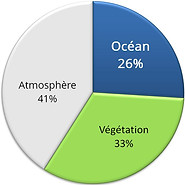
Néanmoins, Il est à peu près certain que le cycle du carbone finira par revenir à un cours naturel et ramener la Terre à une situation stable. La dernière fois, il ne lui a guère fallu que soixante mille ans... C'est un processus très long parce qu'il nécessite à la fois l'utilisation de l'eau de surface et de la tectonique des plaques. en effet, sans tectonique des plaques le système Terre ne donnerait pas le même climat. À titre de comparaison, nous aurions plus un climat ressemblant à celui de Vénus.
Le calcium présent dans les roches sédimentaires a une interaction chimique avec le dioxyde de carbone et influe sur la tectonique des plaques, et ainsi de suite...
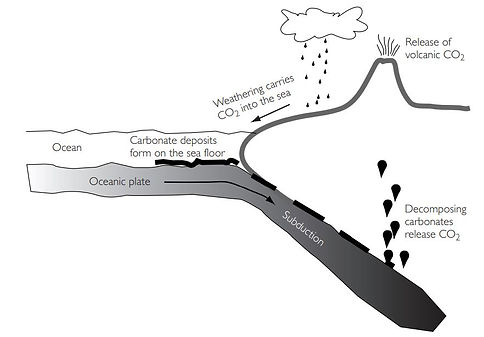
Dans l'océan, le carbone se trouve sous différents formes: le Carbone Inorganique Dissous (DIC) CO2, H2CO3, HCO3 et CO²3. le Carbone Organique Dissout (DOC) molécules organiques> 0,45 um. le Carbone Organique Particulaire (POC). Et les matériaux organiques (fig 3).
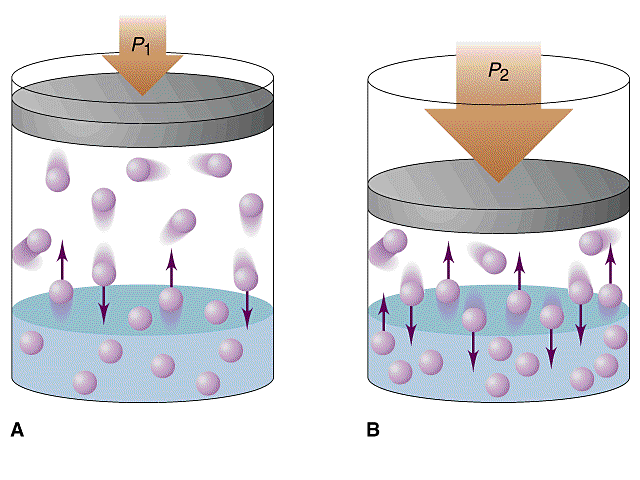
La dissolution des gaz dans les liquides est fixée par la loi de Henry - A température constante, et à saturation, la concentration - C - la quantité de gaz dissous dans un liquide est proportionnelle à la pression partielle - P -qu'exerce ce gaz sur le liquide. Autrement dit, si vous prenez un récipient à moitié plein d'eau et doublez la quantité d'air en pressurisant l'espace d'air, alors deux fois plus de chaque composant dans l'air est absorbé. Que l'on écrit :
P = C . H
Et H est le coefficient de Henry pour le gaz dissous
À chaque instant un pourcentage constant des molécules du gaz dissous dans la phase liquide repasse à l’état gazeux et s’échappe du liquide mais dans le même temps le même pourcentage des molécules de ce gaz passe en solution. Lorsque les deux flux se compensent, l’équilibre de saturation est atteint, soit pour le dioxyde de carbone : CO2 (g) CO2 (aq) c'est important parce que la dissolution des gaz est exothermique (qui dégage de la chaleur), cela signifie que leur solubilité (capacité d'une substance, appelée soluté, à se dissoudre dans une autre substance) diminue avec l'augmentation de la température. Ainsi, la hausse des températures océaniques signifie des niveaux plus faibles d'O2 dissous. Ce qui est problématique pour la vie marine et plus principalement pour les poissons.
Afin de mieux comprendre le mécanisme, une expérience très facile est de mettre une casserole d'eau à chauffer. Avant que l'eau ne commence à bouillir, de petites bulles se forment au fond de la casserole. C'est l'air dissous qui veut sortir de l'eau. Lorsque vous augmentez la température, la solubilité diminue et le gaz sort vers l'atmosphère pour stabiliser le mélange.
Plus fun, ouvrez une canette de soda ( ou de bière) très froide et une canette très chaude et remarquez la différence de solubilité du CO2 dans les deux.
On constate que la loi de Henry dépend de la température et a de grandes implications pour les différences régionales dans l'acidification des océans . C'est donc, la pression partielle du CO2 dans l'atmosphère qui fixe la quantité maximale de CO2 dissous dans les eaux de surface de l'océan.
Dans les faits, certaines régions de l'océan dégazent du CO2 vers l'atmosphère parce que la pression partielle dans l'eau est supérieur à celle de l'atmosphère.
Est ce que les CFC 11 peuvent avoir un impact supplémentaire sur le climat dans les nées à venir ?

Sources et références
https://www.whoi.edu/oceanus/feature/the-rain-of-ocean-particles-and-earths-carbon-cycle/
http://adsabs.harvard.edu/pdf/1993AREPS..21..227H
Bauer, J., Cai, WJ., Raymond, P. et al. Le cycle changeant du carbone de l'océan côtier. Nature 504, 61–70 (2013). https://doi.org/10.1038/nature12857
https://keelingcurve.ucsd.edu/
REDFIELD, ALFRED C. “THE BIOLOGICAL CONTROL OF CHEMICAL FACTORS IN THE ENVIRONMENT.” American Scientist, vol. 46, no. 3, 1958, pp. 230A–221. JSTOR, www.jstor.org/stable/27827150. Accessed 21 Mar. 2021.
Rhein, M., et al., 2013, `` Observations: Ocean '', dans: Climate change 2013: The physical science base. Contribution du Groupe de travail I au cinquième rapport d'évaluation du Groupe d'experts intergouvernemental sur l'évolution du climat, Stocker, TF, et al. (eds), Cambridge University Press, Cambridge, Royaume-Uni, et New York, NY, p. 255-316 ( http://www.climatechange2013.org/images/report/WG1AR5_Chapter03_FINAL.pdf
Forster, PMF et Taylor, KE ( 2006 ). Forcings climatiques et sensibilités climatiques diagnostiqués à partir d'intégrations couplées de modèles climatiques . Journal of Climate , 19 ( 23 ), 6181 - 6194 . https://doi.org/10.1175/JCLI3974.1
Zhang, K. , Wan, H. , Liu, X. , Ghan, SJ , Kooperman, GJ , Ma, PL , Rasch, PJ , Neubauer, D. , et Lohmann, U. ( 2014 ). Note technique: sur l'utilisation du nudging pour les études d'intercomparaison des modèles aérosols-climat . Chimie et physique atmosphériques , 14 ( 16 ), 8631 - 8645 . https://doi.org/10.5194/acp‐14‐8631‐2014
Scott C. Doney, 1 Victoria J. Fabry, 2 Richard A. Feely, 3 et Joan A. Kleypas 4
Acidification des océans: l'autre problème du CO 2
Revue annuelle des sciences marines
Vol. 1: 169-192 (date de publication du volume janvier 2009)
Première publication en ligne en tant que Review in Advance le 29 août 2008
https://doi.org/10.1146/annurev.marine.010908.163834
Bopp, L., Resplandy, L., Orr, JC, Doney, SC, Dunne, JP, Gehlen, M., Halloran, P., Heinze, C., Ilyina, T., Séférian, R., Tjiputra, J ., and Vichi, M .: Multiple stressors of ocean écosystems in the 21st century: projections with CMIP5 models, Biogeosciences, 10, 6225–6245, https://doi.org/10.5194/bg-10-6225-2013, 2013 .
https://www.ipcc.ch/report/ar5/syr/
https://climateilluminated.com/CO2_facts/carbon_cycle/carbonCycle_IPCC_AR5.html

.png)
.png)